
CRISPR-Cas
wykorzystywany jest obecnie przez naukowców do edytowania genów. Swoją medialną
sławę zawdzięcza temu, że jest bardzo kontrowersyjnym tematem, rozpalającym
debaty etyczno-filozoficzno-religijne o „Zabawie w Boga”. Dzięki CRISPR to co
kiedyś było science-fiction, np. modyfikowanie genetycznie ludzkich zarodków,
wskrzeszanie zmarłych gatunków, tworzenie syntetycznego życia czy też pokonanie
malarii poprzez pozbycie się komarów malarycznych, stało się realnymi
dylematami etycznymi, z którymi musimy się teraz zmierzyć.
krok po kroku jak został on odkryty, a pamiętać należy, że było to wynikiem
badań wielu naukowców z całego świata. Komórki naszego ciała zawierają w sobie
cząsteczkę DNA, która składa się z sekwencji nukleotydów. Ta sekwencja
odpowiada za budowę naszego ciała, o czym wiemy od ponad pół wieku. Z czasem
naukowcy nauczyli się coraz lepiej odczytywać sekwencję DNA, czego wielkim
przykładem był Projekt Poznania Ludzkiego Genomu (Human Genome Project), ukończony w 2005 roku. Człowiek nie jest jednak jedyną
istotą której genom został odczytany. Naukowcy zbadali też sekwencje DNA innych
zwierząt, roślin, grzybów, protistów, archeanów, bakterii, wirusów.
pierwszy świadomie zwrócił uwagę na coś bardzo dziwnego w sekwencji DNA
jednego z analizowanych przez niego mikroorganizmów. Podczas badania genomu
kochającego sól mikroba o nazwie Haloferax
mediterranei, dostrzegł w nim 14 regularnie powtarzających się sekwencji
DNA. Każda z tych sekwencji liczyła sobie 30 nukleotydów przy czym były one
palindromiczne, czyli dało się je odczytać normalnie, jak i wspak. Te
powtarzające się sekwencje rozdzielało 35 nukleotydów pozornie losowej
sekwencji DNA, którą nazwał „rozdzielaczem” (ang. spacer). Taka regularna
budowa fragmentu DNA sugerowała, że dzieje się tam coś ciekawego. Francisco
Mojica wysunął hipotezę dotyczącą roli tego miejsca, która jednak szybko
okazała się błędna i zagadka nadal czekała na rozwiązanie. Postanowił swoimi
przemyśleniami podzielić się z innym badaczem: Ruudem Jansenem.
Jest to akronim słów „Clustered Regularly Interspaced Short Palindromic Repeats” czyli po polsku „zgrupowane, regularnie przerywane, krótkie
powtórzenia palindromiczne”. Badacze odkryli, że ta genetyczna anomalia nie
jest odosobnionym przypadkiem. Już w 1987 roku, na podobną sytuację natrafił
przypadkiem Yoshizumi Ishino, który badał sekwencję
jednego z genów bakterii pałeczki okrężnicy. Nie wiedział jednak wówczas za co
odpowiedzialny był ten fragment. Gdy naukowcy z całego świata wiedzieli już
czego szukać, szybko się okazało, że CRISPR jest czymś powszechnym, chociaż
fragmenty te mogą się między sobą różnić u różnych gatunków. Zagadkę funkcji
CRISPR jeszcze bardziej skomplikowało odkrycie, że zaraz przy nich zawsze
znajduje się gen, który tworzył białko o nieznanej funkcji. Gen ten nazwano „Cas”
od skrócenia słów „system skojarzony z CRISPR”.
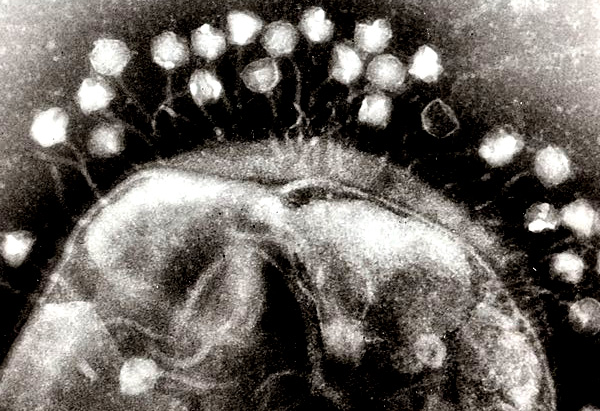
badaczy odkryły coś ważnego. Owe „losowe” fragmenty DNA, które stanowiły
wypełnienie CRISPR wcale nie były przypadkowe. Wiele z nich to genomy wirusów
wbudowane w genomy bakterii. Zatem CRISPR/Cas przypomina zasadniczo więzienie
dla obcego DNA. Pierwotnie odkryte regularne, krótkie, palindromiczne fragmenty
stanowią niejako celę, w której przetrzymywane są pofragmentowane genomy
wirusów. Białko Cas byłoby w tej analogii strażnikiem.
 |
| Savas Abadsidis, https://www.hivplusmag.com |
Tylko po co to więzienie? W 2006 roku Eugene Koonin zaproponował
hipotezę, w której to CRISPR/Cas stanowi „pamięć” komórki o wrogach, którzy
próbowali ją zabić. Posiadając i aktualizując swoistą „bazę danych wirusów”
komórki mogą posiadać swój własny układ odpornościowy. W 2007 roku dwóch
mikrobiologów Rodolphe Barrangou oraz Philippe Horvath pracujących dla firmy
produkującej jogurty, postanowili to sprawdzić doświadczalnie. Mieli nadzieję
stworzyć kultury bakterii w jogurcie, które będą odporne na wirusy, zwiększając
przez to zyski firmy. Zainfekowali bakterie jogurtowe wirusami i szukali ich
wirusowego DNA, dodanego do regionu CRISPR u bakterii, które przeżyły. Ku ich
radości,
znaleźli je. Co więcej wykazali, że po usunięciu
fragmentów wirusów z CRISPR, odporność bakterii na nie zostaje zatracona.
Dowodzi to, że CRISPR faktycznie ma znaczenie w „pamięci” immunologicznej.
tysiące naukowców z całego świata starało się odpowiedzieć na to pytanie. Był to
ekscytujący okres dla biologii molekularnej, kiedy nawet zwykły student mógł
dokonać prostego odkrycia, które zrewolucjonizowałoby naszą wiedzę o systemie
CRISPR/Cas. Oto do czego doszli badacze: białko Cas, które zawsze towarzyszy CRISPR
jest „endonukleazą” – enzymem rozkładającym DNA. Czasami nawet na ilustracjach
naukowych białko Cas symbolizowane jest ikoną Pacmana.
zyskało białko Cas-9. Białko Cas może przeciąć nić DNA w dowolnym miejscu, jak
bardzo ostre nożyczki. Takie przecięcie zazwyczaj w zupełności wystarczy, by
zneutralizować zagrożenie jakim są wirusy. Po pofragmentowaniu genomu wirusa na
części instrukcje w nim zawarte stają się nonsensowne (nie do właściwego przez
komórkę odczytania), jak zapis na kartce papieru pocięty w niszczarce.
 |
| National Human Genome Research Institute, z późn. zm. |
dla samej komórki – zjadałoby własne DNA. Cas posiada jednak RNA-przewodnika
(ang. guide-RNA), który trzyma go w
ryzach i naprowadza na właściwe do zniszczenia DNA. Tylko DNA o identycznej
sekwencji liter z matrycą RNA-przewodnika może zostać w ten sposób zniszczone
przez białko Cas. RNA-przewodnik powstaje z fragmentów odczytanych z „więzienia”,
jakim są fragmenty CRISPR. Dokładniej mówiąc, część RNA-przewodnika stanowi fragment
wirusa przechowywany w „celi”, a część jest „identyfikatorem” dla białka Cas –
strażnika (warto zaznaczyć, że ten podział odkryli uczeni Martin Jinek
oraz Krzysztof Chylinski, gdzie ten jest Polakiem).
Edytowanie genomu w inżynierii genetycznej
Korzystając ze zmodyfikowanego systemu CRISPR/Cas-9, naukowiec może
hipotetycznie wyleczyć człowieka z jego choroby genetycznej. Zasada działania
jest taka sama: wystarczy komórkom człowieka dostarczyć system CRISPR/Cas-9 z
genem, który chcemy wyłączyć, a on ten gen sam znajdzie i zneutralizuje. Co
więcej, gen też można nie tylko przeciąć, ale i zmodyfikować na dowolne
sposoby. Zmienianym komórkom dostarcza się wtedy gen wcześniej zsyntezowany w
laboratorium, a mechanizmy naprawy DNA wklejają fragment w miejsce cięcia
dokonanego przez białko Cas.
na tym, że jest ona tania, wydajna, łatwa w użyciu, szybka, ustandaryzowana i
będzie działać w prawie każdym organizmie. Jednak najważniejsze jest to, że
działa precyzyjniej, niż skalpel. Inżynieria genetyczna wymagała kiedyś miesięcy,
a nawet lat pracy. Teraz z systemem CRISPR/Cas-9 w dwa tygodnie można stworzyć
genetycznie zmodyfikowane ludzkie komórki. Tak się już dzieje. W 2014 roku naukowcom
udało się w ten sposób usunąć wirusa HIV z ludzkich białych krwinek. W 2015 roku stworzono tą metodą komara, który nie przenosi
malarii. Natomiast rok później inna grupa badawcza z Chin, korzystając z
systemu CRISPR/Cas zmodyfikowała ludzkie embriony, „ucząc” ich układ
immunologiczny rozpoznawać komórki złośliwego raka płuc.
CRISPR wszczepił sobie gen, który miał zwiększać jego masę
mięśniową. W tym roku prawdopodobnie rozpoczną się pierwsze badania kliniczne z
wykorzystaniem CRISPR na ludziach. Co więcej, technologia CRISPR dynamicznie
się rozwija i będziemy o niej słyszeć coraz częściej. Już teraz wiemy, że
edytowanie genów to tylko wierzchołek góry lodowej możliwości CRISPR










Świetny artykuł, omawia podstawy, historię, jak i możliwości rozwoju CRISPR-Cas. Pierwszy raz zetknąłem się z ta nazwą w książce Helisa Marca Elsberga.
Pozdrawiam
Tylko patrzeć jak kościółek i różnorakie bioetyczne szumowiny będą chcieli tego zakazać. Dobrze, że metoda jest prosta i tania, miejmy nadzieję, że tego nie da się już zatrzymać, tak jak internetu.
Jako "kościółkowiec" i "szumowina bioetyczna" mam nadzieję ze za pomocą tej metody uda się u ciebie odtworzyć tkankę mózgową. Czy powróci z nią rozum? Tego nie wiem.
I co z tym "biohakerem"? Przypakował się jak Arnold,czy zamienił w "biokompost?"
Taki super wynalazek że będzie mógł niszczyć także dobre DNA. I jak zwykle większość populacji wierzy że będzie on użyty tylko w dobrej wierze.HAHAHAHAHAHAHAHHAHaaaaaa
Ten biohaker to Josiah Zayner i jeszcze nie zakończył eksperymentu z mięśniami. Odsyłam do artykułu pt. "Jak zhakować DNA we własnym domu?"z nr 2/2018 Świata Wiedzy 😉 główne niebezpieczeństwo polega na tym,że taki domorosły biohaker może zmodyfikować dowolny szczep bakterii i uwolnić bo do środowiska co może mieć opłakane konsekwencje…
Zgadzam się w zupełności.Jak zwykle przy jakimś nowym odkryciu mało się mówi o jego niebezpieczeństwach i ich zapobieganiu.
Świetny tekst, przeczytałam jednym tchem!
Bardzo przystępne omówienie odkrycia, które stanowi rewolucję w badaniach nad terapią genową. Drobna korekta: cząsteczek guide-RNA używa się w eksperymentach wykorzystujących CRISPR-Cas9, natomiast pierwotnie, w komórce bakteryjnej, białko Cas9 wchodzi w interakcję z dwiema cząsteczkami RNA: tracrRNA (cząsteczka pełniąca funkcję strukturalną) oraz crRNA (tutaj znajduje się sekwencja komplementarna do miejsca cięcia w docelowym genomie).
Ale Nobla za Crisper cas9 dostala Dudna nie Chyliski!